Quando si sottrae calore da un bagno di metallo liquido con velocità moderata, la temperatura, dopo aver raggiunto il punto d’inizio solidificazione teorico, la temperatura continua a diminuire senza che il liquido solidifichi.
Dopo un certo sottoraffreddamento (isteresi), la solidificazione incomincia e poi progredisce rapidamente, mentre la temperatura del sistema può risalire o continuare a scendere più lentamente finché non si completa la solidificazione di tutto il metallo liquido disponibile.
Questo può essere spiegato considerando gli atomi del metallo allo stato liquido che si muovono caoticamente e non sono disposti secondo uno schema ordinato. Alla temperatura d’inizio solidificazione, dovrebbero ordinarsi secondo lo schema geometrico caratteristico del reticolo cristallino del metallo solido, generando il primo nucleo di cristallizzazione; tuttavia, la probabilità che ciò avvenga è molto bassa.
Spesso accade che gli atomi non trovino immediatamente la loro giusta disposizione; talvolta formano aggregati di dimensioni insufficienti per l’accrescimento di un cristallo e subito si separano, ritornando alla massa caotica del liquido.
In entrambi i casi, il metallo continua a raffreddarsi senza solidificare, cioè non cristallizza.
Il raffreddamento fa diminuire l’energia cinetica degli atomi che rallentano i loro movimenti vibrazionali rotazionali e transazionali: ciò favorisce la probabilità della nucleazione.
Quando un numero sufficientemente grande di atomi, continuando a disporsi secondo configurazioni diverse, assume quella tipica del reticolo cristallino e raggiunge adeguate dimensioni, si forma il primo nucleo stabile (nucleazione endogena).
Subito dopo altri atomi si depositano sul nucleo, che s’accresce rapidamente (accrescimento).
La rapida formazione dei legami solidi cede una discreta quantità di calore (calore latente di solidificazione), sufficiente per compensarne l’asportazione del raffreddamento e per riscaldare un po’ il sistema, che riduce il proprio sottoraffreddamento.
Se l’asportazione di calore è moderata o piccola, la temperatura può aumentare fin quasi a raggiungere quella di solidificazione in condizioni di raffreddamento lentissimo (quasi equilibrio), altrimenti resta inferiore, fino a solidificazione compiuta.
Da questo punto in poi il comportamento del sistema ritorna normale ed il raffreddamento prosegue regolarmente fino a completamento della solidificazione.
Se l’asportazione di calore è elevata, la temperatura scende continuamente, senza evidenziare il tipico arresto alla temperatura di solidificazione del metallo puro in condizioni di raffreddamento lentissimo.
Per ridurre il fenomeno del sottoraffreddamento e favorire la solidificazione si usa l’inoculazione o nucleazione esogena. In tal caso, s’introducono nel liquido minutissimi cristalli di qualsiasi sostanza solida, ala temperatura del liquido, che fungono da inneschi o da germi di cristallizzazione.
Quando la polvere del solido inoculante è di composizione identica a quella del metallo liquido che intendiamo far solidificare più agevolmente, la nucleazioneesogenasi diceomogenea. Se la polvere solida è una sostanza diversa, la nucleazione esogena si diceeterogenea. Anche quest’ultima favorisce la solidificazione, perché gli atomi del liquido sottoraffreddato aderiscono alla superficie solida delle particelle esogene per adsorbimento e sono trattenute, trovando più agevolmente la corretta configurazione cristallina.
Se la velocità di raffreddamento è straordinariamente elevata, anche i metalli non cristallizzano più, ma raggiungono uno stato metastabile di sottoraffreddamento. Gli atomi non hanno più sufficiente energia per traslare e rimangono bloccati mantenendo la disposizione disordinata del liquido (stato amorfo). Si ottengono così i metalli vetrosi o vetri metallici. Essi possiedono alcune proprietà in comune con i solidi, per esempio la rigidità, perciò non sembra appropriato definirli fluidi eccezionalmente viscosi.
Con la diffrattometria ai raggi X, tecnica che consente di studiare la disposizione dei piani atomici nelle sostanze cristalline, si ottengono diffrattogrammi sfocati, o con aloni, che dimostrano una disposizione caotica degli atomi, molto diversa da quella dei solidi cristallini, dove i diversi piani atomici generano numerose macchie, particolarmente ordinate e ben focalizzate (figura 1).

Nei solidi amorfi i piani atomici non esistono e gli spettri di diffrazione non generano macchie, se non molto sfumate e confuse, in posizioni irregolari, come accade per tutti i liquidi.
In casi rarissimi e ricorrendo a tecniche particolari, nel liquido sottoraffreddato è possibile formare un unico germe di cristallizzazione. A solidificazione ultimata s’ottiene un monocristallo che occupa l’intero volume del solido, con forma uguale a quella del recipiente che conteneva il liquido.
Durante la solidificazione reale, nella massa liquida sottoraffreddata si formano germi di cristallizzazione, tanto più numerosi quanto maggiore è il sottoraffreddamento prima della nucleazione. Essi s’accrescono indipendentemente l’uno dall’altro, finché vengono a contatto con l’esaurirsi del liquido.
Se non esistono condizioni di solidificazione particolari, che favoriscono l’orientamento, i cristalli si dispongono in modo casuale, generando una cristallizzazione equiassica, dove, in ogni direzione, esiste un numero uguale di cristalli orientati nello stesso modo.
La solidificazione avviene sempre in direzione opposta alla fuga del calore, cioè dalla parete del contenitore (lingottiera) verso il nucleo del lingotto.
In condizioni di scarsa nucleazione (basse velocità di raffreddamento o sottoraffreddamento piccolo o nullo), i cristalli già solidificati a contatto con la superficie fredda della lingottiera, s’accrescono perpendicolarmente alla parete, generando una cristallizzazione orientata o cristallizzazione colonnare.
La macrostruttura di solidificazione, tipica di un lingotto quadro, è quella schematizzata in figura 2, dove si osserva: un sottile guscio superficiale con cristallizzazione equiassica finissima; uno strato intermedio con cristallizzazione colonnare, più o meno estesa; il nucleo con cristallizzazione equiassica grossolana.
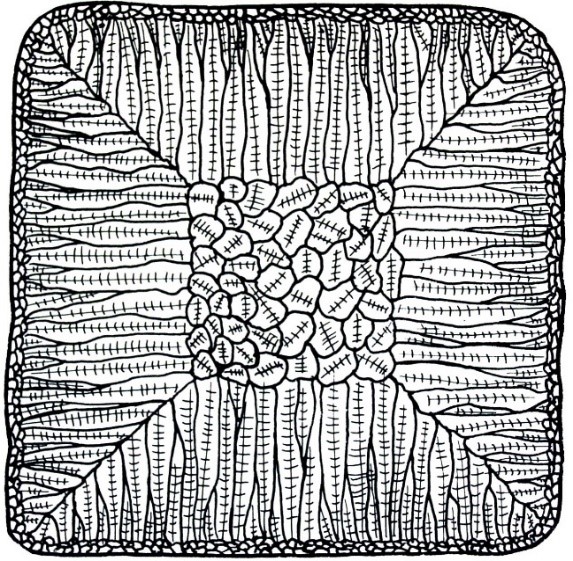
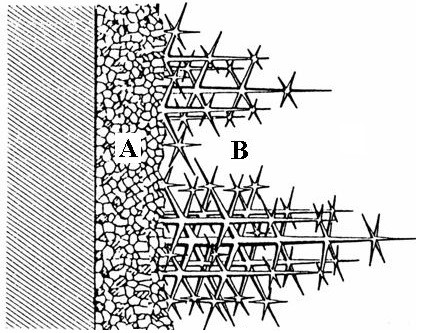
Il primo strato si forma in condizioni di grande sottoraffreddamento, perché non appena il liquido tocca la superficie della lingottiera, si raffredda rapidamente e genera moltissimi nuclei di cristallizzazione, il cui accrescimento s’arresta rapidamente per mutuo contatto. Si forma così la pelle del lingotto caratterizzata da finissima cristallizzazione, senza orientamento preferenziale (zona A di figura 3).
Il guscio solido appena formato si stacca dalla lingottiera, per contrazione termica; così, il calore non è più smaltito per conduzione attraverso il contatto diretto tra lingotto e lingottiera, ma per convezione ed irraggiamento attraverso l’aria che divide le due superfici: perciò la velocità di raffreddamento cade bruscamente. Il sottoraffreddamento si riduce al minimo o s’annulla e blocca la nucleazione di altri cristalli.
La solidificazione continua per accrescimento dei cristalli del guscio superficiale affacciati al liquido, che si sviluppano verso l’interno, allungandosi notevolmente e generando la cristallizzazione orientata, o colonnare (zona B di figura 3).
Quando i cristalli diventano sufficientemente lunghi da ondeggiare nel liquido residuo, soggetto a moti convettivi, si possono rompere in piccoli frammenti, che si disperdono nel liquido residuo e diventano nuclei d’accrescimento di altrettanti cristalli. Essi solidificano con orientamento casuale (cristallizzazione equiassica) nel liquido residuo, cioè nella parte più interna del lingotto (parte centrale di figura 2).
CRISTALLIZZAZIONE DENDRITICA
L’accrescimento dei cristalli avviene sempre con l’apporto di nuovi atomi che si dispongono sulle facce del cristallo già solidificato, come per accostamento di nuove celle elementari al reticolo cristallino del nucleo originario.
Per varie ragioni l’accrescimento si manifesta in una direzione preferenziale. Si sviluppano così strutture arborescenti dette dentriti (figure 4 e 5), costituite da un tronco, rami principali, su cui s’accrescono rami secondari e terziari, che formano fra loro angoli tipici della simmetria del cristallo.
Nel caso delle leghe ferrose sempre con simmetria cubica, tutti gli angoli sono retti.
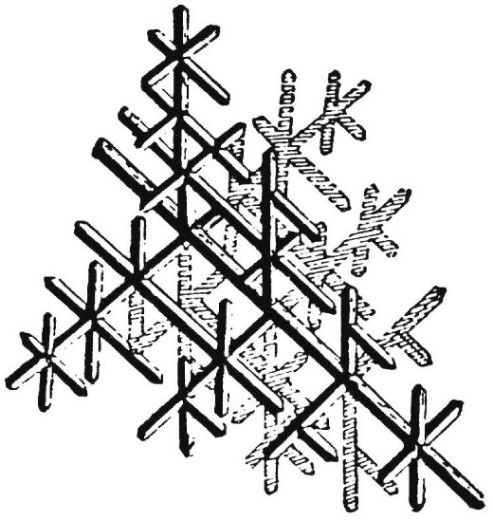

Durante la solidificazione i singoli rami s’accresceranno dimensionalmente, ingrossandosi fino a completa solidificazione dell’intero cristallo, colmando ogni spazio tra loro.
Dalla lezione del 12 Novembre 2020 “Metallurgia fondamentale delle leghe metalliche”
Cesare Cibaldi, Docente AQM area Metallurgia






